5月(yuè)28日,上海市衛健委監督所官方網站公布了(le)“腫瘤治療黑(hēi)幕”涉事醫生陸巍的(de)相關處罰結果。處罰信息顯示,對(duì)陸巍處以“警告,罰款人(rén)民币叁萬元整,暫停執業6個(gè)月(yuè)”的(de)處罰。處罰的(de)事由爲“未按規定填寫病曆資料,提供醫療衛生服務過程中未按照(zhào)規定履行告知義務”。對(duì)上海交通(tōng)大(dà)學醫學院附屬新華醫院處以“警告,罰款人(rén)民币肆萬元整”的(de)處罰。處罰事由是:醫療機構醫療質量管理(lǐ)不健全。
并且,因“未取得(de)醫療機構執業許可(kě)證擅自執業”,上海嘉慷生物(wù)工程有限公司被處以“處罰沒收違法所得(de)15萬元,罰款人(rén)民币150萬元;罰沒款合計165萬元”的(de)處罰。
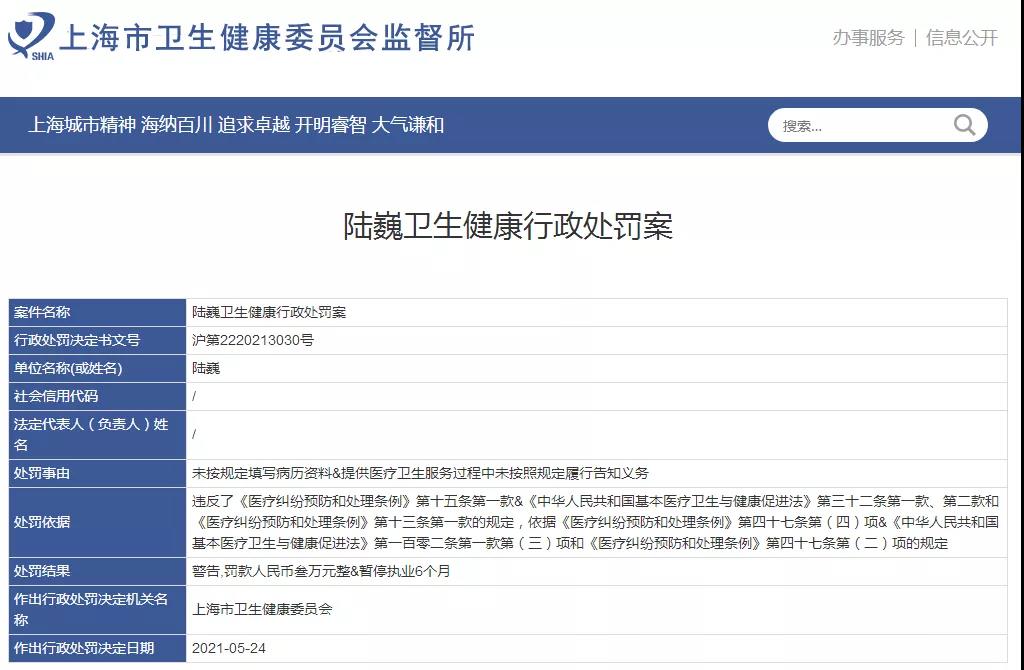
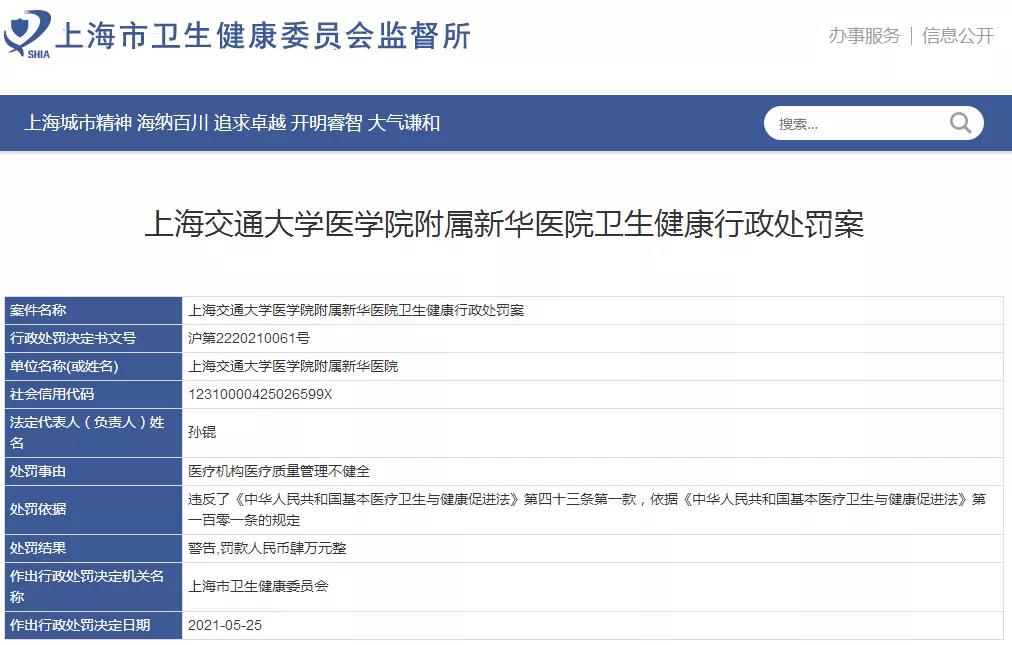
4月(yuè)18日晚,北(běi)京大(dà)學第三醫院醫生張煜在某平台發表一篇題爲《寫給我摯愛(ài)的(de)國家和(hé)衆多(duō)的(de)腫瘤患者和(hé)家屬——請與我一起呼籲,請求國家盡早設立醫療紅線,遏制腫瘤治療中的(de)不良醫療行爲》的(de)推文。文中指出上海某三甲醫院普外科醫生陸巍蓄意誘導治療,導緻患者馬進倉花費了(le)常規治療10倍以上的(de)資金,其中包括做(zuò)NGS基因測序,接受了(le)“NK細胞療法”、濫用(yòng)輔助用(yòng)藥等,結果人(rén)财兩空。
對(duì)于此次事件的(de)處理(lǐ)結果,雖然涉事醫生、醫院和(hé)企業都受到了(le)處罰,但仍有許多(duō)問題沒有得(de)到解決,醫生與細胞公司之間是否有利益輸送?醫院對(duì)這(zhè)些事是否知情?這(zhè)些混亂是怎麽造成的(de)?如何解決?
究竟什(shén)麽是細胞療法?
是“收割患者”,還(hái)是“一線希望”
張煜醫生的(de)發文讓細胞療法再一次走進大(dà)衆視野。
細胞治療是利用(yòng)患者自體(或異體)的(de)成體細胞(或幹細胞)經過生物(wù)工程改造,移植或者輸入患者體内,對(duì)組織、器官進行修複的(de)治療方法。
按照(zhào)細胞種類,細胞療法可(kě)以分(fēn)爲幹細胞治療和(hé)免疫細胞治療,前者廣泛應用(yòng)于血液類疾病、器官移植、心血管系統疾病、肝髒疾病、神經系統疾病、組織創傷等疾病領域。
細胞免疫治療療法包括CAR-T細胞治療、CIK細胞治療、DC-CIK細胞治療、DC細胞治療、NKT細胞治療、ACTL細胞治療等。其中,CAR-T細胞治療全稱嵌合抗原受體T細胞治療,是免疫細胞療法中最有希望攻克腫瘤的(de)療法。目前,全球已有5款CAR-T細胞療法獲FDA批準上市。
對(duì)于張煜醫生提到的(de)NK細胞療法是指通(tōng)過采血,提取患者體内的(de)免疫細胞,進行體外擴增後,再回輸注回患者體内,以增強患者免疫力,殺傷腫瘤細胞。但該療法的(de)療效還(hái)未得(de)到驗證,還(hái)屬于臨床研究階段。此前,魏則西生前接受了(le)DC-CIK細胞治療,也(yě)還(hái)停留在早期臨床研究階段。
盡管NK療法沒有獲批用(yòng)于臨床,但不少從事NK細胞療法業務的(de)企業商人(rén)逐利而行轉入地下(xià),形成一條龐大(dà)的(de)灰色産業鏈。治療價格更是亂象疊出,一針價格從幾萬到幾十萬不等,一個(gè)療程費用(yòng)可(kě)達上百萬元。
根據藥智輿情大(dà)數據監控系統顯示,自4月(yuè)18日張煜醫生發文以來(lái),”細胞治療“相關話(huà)題呈現高(gāo)度輿情熱(rè)度,截至目前,相關數據總量113936條,輿情演化(huà)過程呈現出如下(xià)特點:
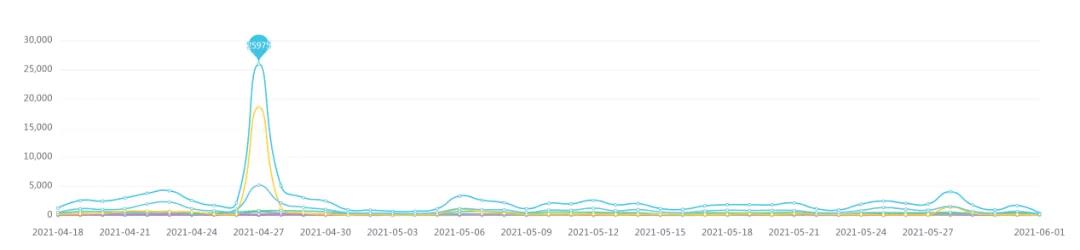
信息來(lái)源走勢圖

關鍵詞雲
對(duì)“細胞治療”話(huà)題比較關注的(de)除了(le)行業人(rén)員(yuán)及進行相關行業投資者,還(hái)有腫瘤等難治性疾病患者及患者家屬。一些非法售賣細胞産品者在各社群鼓吹細胞治療效果,讓一些腫瘤患者或其家屬相信,細胞療法是“放手一搏”的(de)機會。再引導其私下(xià)交易,重金購(gòu)買他(tā)們的(de)産品,患者最終可(kě)能得(de)到了(le)一定的(de)治療效果,但更可(kě)能是人(rén)财兩空。
雖然CAR-T、NK細胞療法等療法是當下(xià)研發的(de)熱(rè)點,但國内目前尚無細胞免疫療法獲批上市。國内進度最快(kuài)的(de)産品是上海複星醫藥與美(měi)國吉利德旗下(xià)Kite Pharma成立的(de)合資企業複星凱特的(de)阿基侖賽注射液,其上市申請已于今年1月(yuè)進入行政審批階段,但至今仍未獲批。
而地下(xià)産業的(de)細胞産品根本無法保證療效。對(duì)于求醫心切的(de)患者,可(kě)以關注正規臨床試驗,對(duì)于符合入組條件的(de)可(kě)以申請試藥。
細胞治療亂象原因何在?
宜明(míng)細胞質量總裁劉雙生認爲,“現在衛健委監管的(de)缺失是造成混亂現狀的(de)主要原因。體細胞非法臨床用(yòng)藥黑(hēi)幕問題并非上海特有,其它地區(qū)也(yě)存在。北(běi)京大(dà)學第三醫院腫瘤化(huà)療科主治醫師張煜先生是一個(gè)警示此類違法行爲的(de)吹哨者。”
近年來(lái),細胞/基因等新技術發展的(de)非常快(kuài),需要新的(de)法規支持。自2009年衛生部将基因治療歸入第三類醫療技術目錄開始,衛生部的(de)監管缺失造成基因、細胞治療産品從此開始進入混亂的(de)無序狀态。魏則西事件終止了(le)這(zhè)種亂象,也(yě)使細胞治療發展陷入低迷狀态。2017年諾華的(de)CAR-T産品獲批上市,重新引起從業者和(hé)監管機構的(de)重視。CDE的(de)介入使基因和(hé)免疫細胞治療産品的(de)監管得(de)到有序發展。
但是衛健委出台的(de)兩個(gè)文件,《生物(wù)醫學新技術臨床應用(yòng)管理(lǐ)條件(征求意見稿》和(hé)《體細胞治療臨床研究和(hé)轉化(huà)應用(yòng)管理(lǐ)辦法(試行)(征求意見稿)》(征求意見稿)又給了(le)一些企業不願走藥監局途徑的(de)企業希望。
劉雙生認爲,雖然衛健委的(de)想法是好的(de),想讓細胞治療技術能快(kuài)速進入臨床使患者受益。但衛健委不能像藥監局那樣擁有完善的(de)審評機制和(hé)現場(chǎng)核查機制,不能像藥監局那樣嚴格監管,導緻衛健委提出的(de)建議(yì)難以落地。
基于這(zhè)兩個(gè)征求意見稿的(de)不确定性和(hé)不可(kě)實施性,目前來(lái)看這(zhè)兩個(gè)文件很可(kě)能已被擱置了(le),細胞治療産品想走第三類醫療技術這(zhè)條路不太現實,但是國家可(kě)能會開個(gè)别口子,例如針對(duì)兒(ér)童罕見病的(de)。但是仍然會要求遵守GMP原則。
我國細胞治療産業發展的(de)主要矛盾是監管體系建設滞後于産業發展速度,國家正在加大(dà)對(duì)細胞治療産業發展的(de)支持力度。目前,研發階段相關指導文件基本已落地,但是缺乏指導NDA上市核查标準的(de)政策落地文件,預計也(yě)将很快(kuài)就會落地。
結語
對(duì)于事件的(de)處理(lǐ)結果,張煜醫生于5月(yuè)28日中午發文表示,對(duì)上述行政處罰決定感到“五味雜(zá)陳,難以評價”。他(tā)寫道,“我的(de)願望很簡單:希望民衆能得(de)到規範的(de)醫療,不良醫療行爲越來(lái)越少。以及我的(de)很多(duō)同道,那些踏踏實實爲患者健康努力的(de)醫生,能夠勞有所得(de)。”
細胞治療在腫瘤、免疫性疾病、神經系統疾病、慢(màn)性病及罕見病等領域展現了(le)良好的(de)應用(yòng)前景,是當下(xià)生物(wù)醫藥研發最熱(rè)門的(de)賽道之一。一方面,細胞治療爲疾病治愈帶來(lái)了(le)希望,另一方面,利益的(de)驅使讓這(zhè)個(gè)行業變得(de)混亂。非法使用(yòng)細胞産品者打亂了(le)市場(chǎng),打擊了(le)正常研究申報者的(de)信心。唯有健全監管機制,規範細胞治療産品研究、臨床試驗及商業化(huà)才能真正造福患者。
----------THE END----------
免責聲明(míng):本文系轉載分(fēn)享,文章(zhāng)觀點、内容、圖片及版權歸原作者所有,如涉及侵權請聯系删除!