至今還(hái)清晰記得(de)報考研究生選專業的(de)時(shí)候自己非常堅決地選擇了(le)藥物(wù)化(huà)學,在我當時(shí)有限的(de)書(shū)本知識範圍裏,小分(fēn)子靶向藥物(wù)的(de)春天就要來(lái)了(le),而我蠢蠢欲動,想做(zuò)那“站在風口的(de)豬”。研究生入學是2014年,也(yě)正是PD-1單抗上市的(de)元年,BMS的(de)Opdivo(O藥)與MSD的(de)Keytruda(K藥)相繼成功上市,并以摧枯拉朽之勢迅速拿下(xià)多(duō)個(gè)腫瘤适應症。再到後來(lái)基因療法、細胞療法等多(duō)種創新生物(wù)技術的(de)層出不窮,我想可(kě)能很多(duō)從事小分(fēn)子藥物(wù)研發的(de)人(rén)和(hé)我一樣如坐(zuò)針氈,這(zhè)也(yě)迫使我在五年研究生階段一直到後來(lái)參加工作都在思考小分(fēn)子藥物(wù)“尚能飯否”這(zhè)個(gè)問題。關于這(zhè)個(gè)問題,我和(hé)同學、同事以及導師都有過多(duō)次激烈的(de)討(tǎo)論,終究也(yě)沒有誰能完全說服對(duì)方,小分(fēn)子藥物(wù)與生物(wù)創新療法(包括抗體、基因療法、細胞療法等)的(de)博弈,到底是“愈久彌香”還(hái)是“長(cháng)江後浪拍(pāi)前浪”,我想結論還(hái)是留給時(shí)間來(lái)檢驗。
一、小分(fēn)子藥物(wù)的(de)困境—“前狼後虎”
回顧創新藥近20年的(de)銷售數據,我們發現在2000年全球銷售額Top10創新藥中8個(gè)爲小分(fēn)子藥物(wù),從2008年開始Top10銷售額創新藥中的(de)小分(fēn)子藥物(wù)開始小于等于5個(gè),到2019年Top10中僅有4個(gè)爲小分(fēn)子,小分(fēn)子藥物(wù)逐步失去了(le)銷售額的(de)頭把交椅,在整體銷售額中的(de)占比也(yě)呈現逐步下(xià)降趨勢。在衆多(duō)潛力生物(wù)技術療法的(de)沖擊下(xià),小分(fēn)子藥物(wù)的(de)市場(chǎng)正在逐步被侵蝕,更有悲觀者擔憂随著(zhe)層出不窮生物(wù)療法的(de)湧現,小分(fēn)子藥物(wù)是否可(kě)能最終逐步退出曆史的(de)舞台。
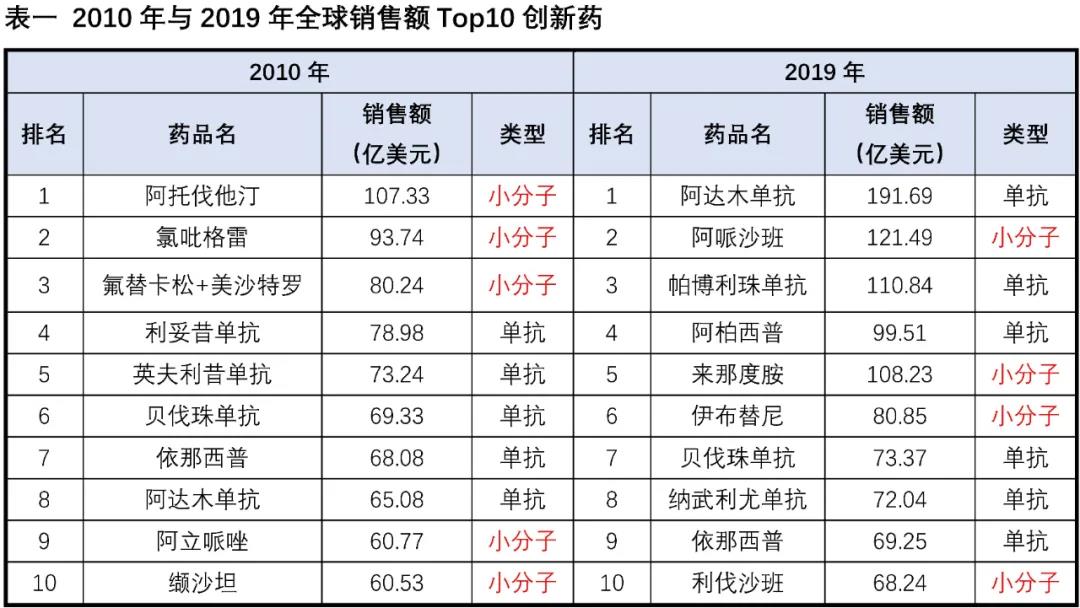
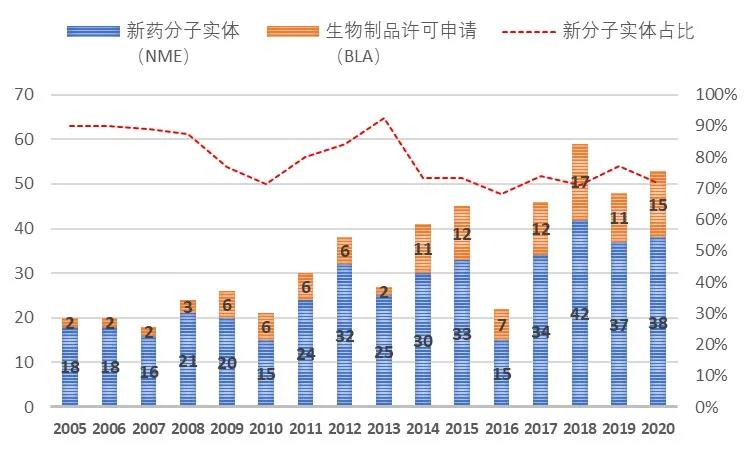
圖1FDA 2005-2020批準新藥
圖片來(lái)源:康橙投資
想要探討(tǎo)小分(fēn)子藥物(wù)自身發展的(de)困境,首先需要了(le)解現代小分(fēn)子藥物(wù)研發最重要的(de)基礎手段-篩選(Screening)。要進行篩選,首先你要有一個(gè)代表某種疾病指征的(de)“篩子”,這(zhè)個(gè)“篩子”可(kě)能是一個(gè)靶點蛋白,也(yě)可(kě)能是一個(gè)細胞株,甚至可(kě)能是一批實驗動物(wù)。其次要有一個(gè)庫(小分(fēn)子library),庫裏面要有足夠的(de)分(fēn)子供你篩選,從相應的(de)庫裏面“大(dà)海撈針”找到一個(gè)或多(duō)個(gè)符合要求的(de)苗頭化(huà)合物(wù)(Hit),經過層層結構優化(huà)得(de)到先導化(huà)合物(wù)(Lead)、候選化(huà)合物(wù)(Candidate),再經過系統的(de)臨床試驗充分(fēn)驗證安全性與有效性,才能得(de)到患者使用(yòng)的(de)藥物(wù)。
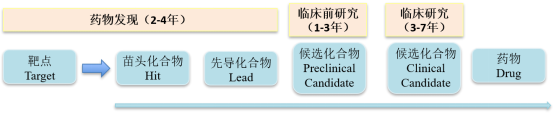
圖2 小分(fēn)子藥物(wù)研發流程
圖片來(lái)源:康橙投資
個(gè)世紀末到本世紀初,小分(fēn)子藥物(wù)研發的(de)突飛(fēi)猛進很大(dà)程度依賴于疾病新靶點和(hé)疾病指征的(de)發現以及有機合成化(huà)學的(de)爆發式發展與各類檢測技術的(de)進步。有機合成化(huà)學從上個(gè)世紀70-80年代開始迎來(lái)爆發,導緻了(le)大(dà)量複雜(zá)、帶有雜(zá)原子的(de)、用(yòng)原有方法很難合成的(de)分(fēn)子的(de)出現;而質譜(MS),核磁共振(NMR)等檢測手段的(de)進步也(yě)導緻了(le)很多(duō)天然産物(wù)的(de)成功分(fēn)離,與此同時(shí)檢測手段的(de)進步也(yě)助推了(le)新靶點的(de)發展(如基因測序、蛋白質組學)。生物(wù)技術的(de)發展導緻了(le)一些重要的(de)疾病指标和(hé)靶點的(de)發現,從而使得(de)各大(dà)制藥公司能夠使用(yòng)手中數百萬計的(de)小分(fēn)子對(duì)這(zhè)些疾病和(hé)靶點進行篩選,進而促使了(le)小分(fēn)子新藥的(de)大(dà)爆發。雖然說小分(fēn)子庫到現在還(hái)在逐年增長(cháng),但是分(fēn)子的(de)類型和(hé)多(duō)樣性的(de)增速卻在逐年降低,促進小分(fēn)子藥物(wù)研發突破的(de)主要還(hái)是新的(de)靶點和(hé)疾病指征的(de)發現。目前大(dà)多(duō)數的(de)公司其實是在用(yòng)新的(de)“篩子”不停地篩舊(jiù)的(de)化(huà)合物(wù)庫,期望那些之前沒有被篩出來(lái)或者已經被篩出來(lái)的(de)分(fēn)子能在新的(de)靶點上起效。當然藥物(wù)化(huà)學家們也(yě)很早期就意識到了(le)這(zhè)個(gè)問題的(de)存在,之後又陸續開發了(le)組合化(huà)學(Combinatorial Chemistry)、DNA編碼化(huà)合物(wù)庫(DNA Encoding Library,DEL)技術來(lái)擴充化(huà)合物(wù)庫。這(zhè)兩種技術在一定階段上緩解了(le)化(huà)合物(wù)庫匮乏的(de)危機,但是它們都依賴于現有的(de)經典有機合成反應,同時(shí)對(duì)反應條件還(hái)有嚴格的(de)要求,受限的(de)化(huà)學反應類型在一定程度上決定了(le)的(de)分(fēn)子種類規模上限,進而影(yǐng)響了(le)化(huà)合物(wù)庫中化(huà)合物(wù)結構的(de)多(duō)樣性。
二、博弈
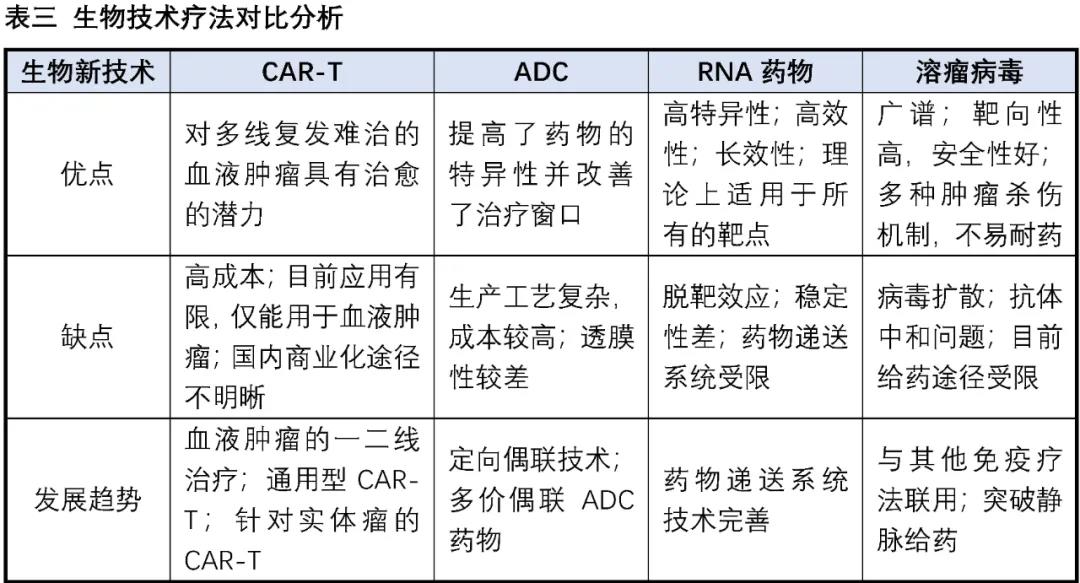
在巨大(dà)的(de)醫藥市場(chǎng)與強大(dà)的(de)社會責任感的(de)驅使下(xià),全球主要經濟體都在竭盡所能努力發展生物(wù)醫藥産業,各種創新生物(wù)技術療法如雨(yǔ)後春筍般湧現,爲廣大(dà)的(de)病患帶來(lái)更多(duō)恢複健康、延長(cháng)壽命的(de)選擇。目前已經有成功上市産品的(de)生物(wù)技術療法包括抗體藥物(wù)、ADC、CAR-T細胞療法、基因療法、RNA藥物(wù)、溶瘤病毒等,其中抗體藥物(wù)的(de)發展最爲成熟,以2019年爲例,銷售額Top10中有6個(gè)爲抗體藥物(wù)。下(xià)表我們以小分(fēn)子藥物(wù)與抗體藥物(wù)的(de)對(duì)比爲例,來(lái)探討(tǎo)小分(fēn)子藥物(wù)與創新生物(wù)技術的(de)優劣勢。
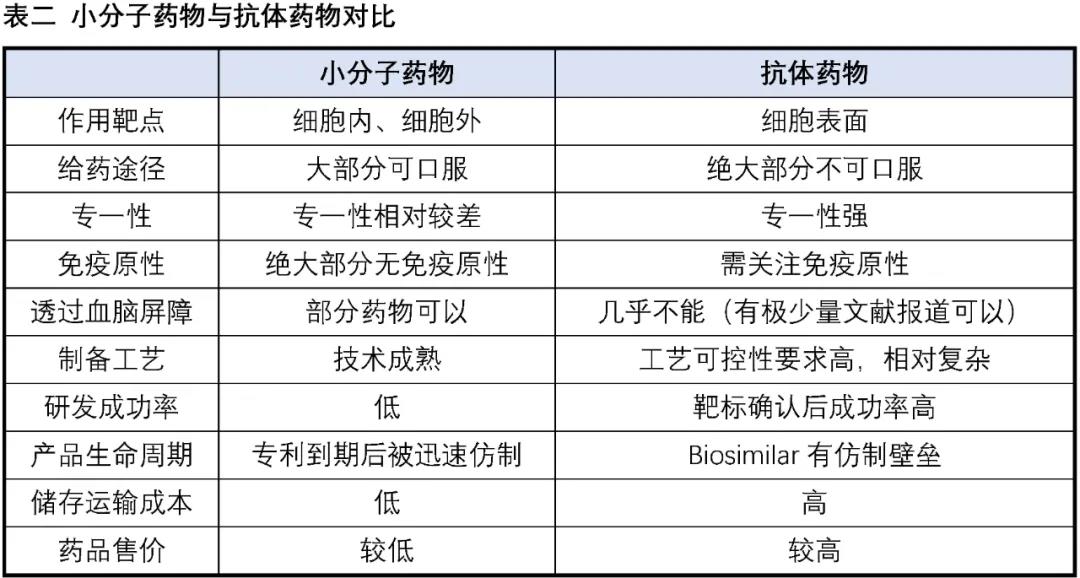
資料來(lái)源:康橙投資
相對(duì)大(dà)分(fēn)子抗體藥物(wù)等生物(wù)技術,小分(fēn)子藥物(wù)的(de)優勢:
(1)大(dà)部分(fēn)的(de)小分(fēn)子藥物(wù)可(kě)以口服,給藥方便,相比之下(xià)絕大(dà)部分(fēn)的(de)生物(wù)技術産品都采用(yòng)注射類給藥方式,患者依從性差。
(2)小分(fēn)子藥物(wù)能很好地作用(yòng)于細胞内(包括細胞核内靶點)與細胞外的(de)靶點。
(3)部分(fēn)小分(fēn)子藥物(wù)能通(tōng)過血腦(nǎo)屏障,可(kě)用(yòng)于腦(nǎo)部疾病治療,目前作用(yòng)于中樞神經體統的(de)藥物(wù)依然以小分(fēn)子爲主。
(4)小分(fēn)子藥物(wù)對(duì)儲存環境的(de)敏感性相對(duì)較低,儲存運輸方便。
(5)幾乎沒有免疫原性,生物(wù)技術産品如抗體、基因治療的(de)AAV病毒等都有可(kě)能被免疫系統識别爲抗原激發免疫反應。
(6)小分(fēn)子藥物(wù)相對(duì)更容易實現差異化(huà),這(zhè)受益于小分(fēn)子藥物(wù)衆多(duō)且相對(duì)成熟的(de)靶點,同時(shí)針對(duì)小分(fēn)子進行的(de)微小改動往往能收獲意向不到的(de)效果(如代謝改善、選擇性提高(gāo)、毒性降低等)。相比之下(xià)生物(wù)技術相關療法的(de)起步相對(duì)較晚,技術相對(duì)不是那麽成熟,從而使得(de)同一技術在相同領域容易出現嚴重的(de)同質化(huà)現象,如“百家争鳴”的(de)PD-1/PD-L1抗體、CD-19-CAR-T細胞療法(這(zhè)兩個(gè)産品的(de)國内臨床試驗登記項目數量都超過了(le)100家)。
相對(duì)大(dà)分(fēn)子抗體藥物(wù)等生物(wù)技術,小分(fēn)子藥物(wù)的(de)劣勢:
(1)對(duì)于沒有适合作用(yòng)口袋的(de)靶點較難開發,比如蛋白質-蛋白質相互作用(yòng)界面一般大(dà)而平坦,沒有很好的(de)口袋容納小分(fēn)子,而利用(yòng)大(dà)分(fēn)子藥物(wù)比如擁有類似作用(yòng)面的(de)抗體來(lái)幹擾卻特别有效。
(2)特異性不高(gāo),小分(fēn)子藥物(wù)由于結構相對(duì)較小,往往容易對(duì)多(duō)個(gè)靶點有活性,這(zhè)也(yě)是許多(duō)小分(fēn)子藥物(wù)副作用(yòng)大(dà)的(de)原因。
(3)半衰期短,往往需要一日一次甚至一日多(duō)次服用(yòng)。
(4)開發成功率較低,以抗體藥物(wù)爲例的(de)整體研發成功率約爲20%,相比之下(xià)小分(fēn)子藥物(wù)整體研發成功率僅爲約11%。
(5)制備工藝相對(duì)簡單成熟。這(zhè)一點既是優勢也(yě)是劣勢,相對(duì)簡單成熟的(de)制備工藝使得(de)小分(fēn)子藥物(wù)的(de)生産成本遠(yuǎn)低于其他(tā)生物(wù)技術産品,同時(shí)正是相對(duì)簡單成熟的(de)制備工藝,當一種小分(fēn)子藥物(wù)的(de)專利到期時(shí),仿制藥能以相對(duì)低廉的(de)成本搶占原研市場(chǎng),造成小分(fēn)子藥物(wù)的(de)“專利懸崖”。
小分(fēn)子藥物(wù)作爲最傳統的(de)藥物(wù)形式,雖然當前的(de)發展遇到一些困境,但也(yě)有其難以替代的(de)優勢。ADC、細胞療法、基因治療等新藥物(wù)形式正在逐步興起,在多(duō)個(gè)治療領域表現自己獨到的(de)優勢和(hé)驚人(rén)的(de)潛力,但同時(shí)也(yě)面臨著(zhe)各自的(de)嚴峻挑戰,相信在不久的(de)将來(lái)也(yě)會是多(duō)種藥物(wù)形式共存的(de)競争格局,各類療法的(de)追随者也(yě)會努力在自己的(de)領域尋求突破。
三、小分(fēn)子的(de)出路—“長(cháng)出一個(gè)小翅膀,就能飛(fēi)得(de)更高(gāo)”
“站在風口上豬都能飛(fēi)起來(lái)”後面其實還(hái)有下(xià)半句—“長(cháng)出一個(gè)小翅膀,就能飛(fēi)得(de)更高(gāo)”。小分(fēn)子藥物(wù)作爲曾經“站在風口的(de)豬”,當前的(de)發展雖然遭遇困境,但是隻要在某些關鍵點做(zuò)出新的(de)突破,爲自己加上一個(gè)小翅膀,我想小分(fēn)子藥物(wù)的(de)未來(lái)當然可(kě)以更高(gāo)更遠(yuǎn)。随著(zhe)分(fēn)子生物(wù)學、結構生物(wù)學的(de)快(kuài)速發展,小分(fēn)子藥物(wù)發現進入基于靶點的(de)藥物(wù)設計的(de)時(shí)代,我們能夠基于某個(gè)靶點進行高(gāo)通(tōng)量篩選,可(kě)以獲得(de)小分(fēn)子和(hé)靶蛋白的(de)複合晶體結構,在計算(suàn)機的(de)輔助下(xià)進行合理(lǐ)優化(huà),藥物(wù)的(de)研發變得(de)如此清晰。高(gāo)通(tōng)量篩選(High Throughput Screening,HTS)、虛拟篩選(Virtual Screening)、基于結構的(de)藥物(wù)設計(Structure-based Drug Design,SBDD)以及基于片段的(de)藥物(wù)設計(Fragment-based Drug Discovery,FBDD)逐漸成爲小分(fēn)子藥物(wù)研發的(de)常見技術。這(zhè)些技術取得(de)了(le)很大(dà)的(de)成功,也(yě)仍然在不斷豐富和(hé)發展中,然而小分(fēn)子藥物(wù)發現的(de)效率并沒有如人(rén)們期待的(de)那樣大(dà)幅提高(gāo)。近幾年小分(fēn)子領域也(yě)在出現諸多(duō)新的(de)思路,實現新的(de)突破,小編認爲小分(fēn)子可(kě)能在如下(xià)幾個(gè)方面實現突破:PROTAC技術、分(fēn)子膠、變構調節、老藥新用(yòng)。
1.PROTAC技術
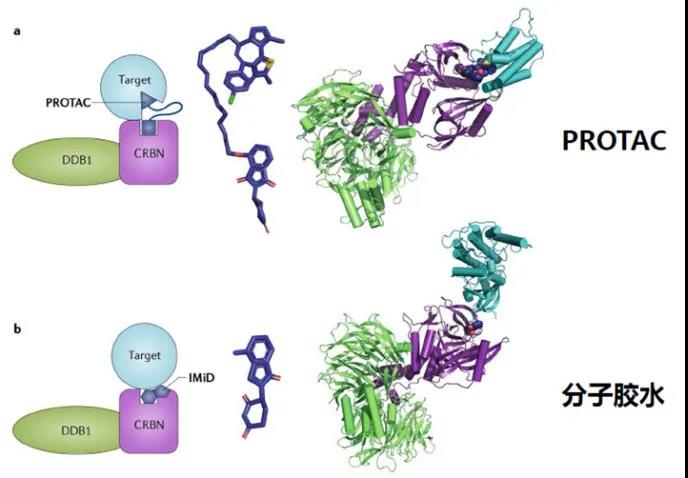
PROTAC(Proteolysis Targeting Chimera,蛋白降解靶向嵌合體)是一種雙功能小分(fēn)子,由靶蛋白配體和(hé)E3泛素連接酶配體通(tōng)過Linker連接得(de)到,利用(yòng)泛素-蛋白酶系統識别、結合并降解疾病相關的(de)靶蛋白。該技術最早由Raymond Deshaies等人(rén)在2001年提出,理(lǐ)論上可(kě)以将任何過表達和(hé)突變的(de)緻病蛋白清除,從而治療疾病。
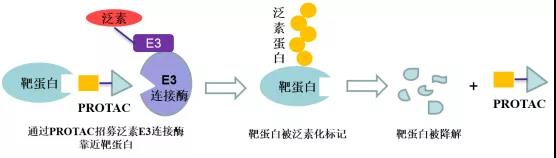
實際在臨床上也(yě)有部分(fēn)藥物(wù)被意外發現具有降解靶蛋白的(de)作用(yòng):比如乳腺癌治療藥物(wù)氟維司群可(kě)以降解雌激素受體;來(lái)那多(duō)胺可(kě)以特異性降解轉錄因子IKZF1和(hé)IKZF3;第三代EGFR抑制劑奧希替尼也(yě)能選擇性誘導EGFR-T790M的(de)降解。這(zhè)些意外的(de)發現沒有普适性,也(yě)較難通(tōng)過合理(lǐ)設計來(lái)得(de)到。PROTAC作爲主觀設計的(de)降解靶标蛋白的(de)小分(fēn)子,在腫瘤、自身免疫性疾病領域已經取得(de)了(le)驚人(rén)的(de)進展,同時(shí)在“不可(kě)成藥靶點”與當前療法耐藥患者治療中表現出巨大(dà)的(de)潛力,獲得(de)了(le)科學界和(hé)資本市場(chǎng)的(de)廣泛認可(kě),目前已有多(duō)家PROTAC公司登陸納斯達克,多(duō)家跨國藥企也(yě)積極參與布局該賽道,達成了(le)多(duō)筆重磅合作協議(yì)。PROTAC技術戴著(zhe)“明(míng)星光(guāng)環”前行,是否能夠帶領小分(fēn)子藥物(wù)再度崛起,取決于未來(lái)幾年相關産品的(de)臨床進展。
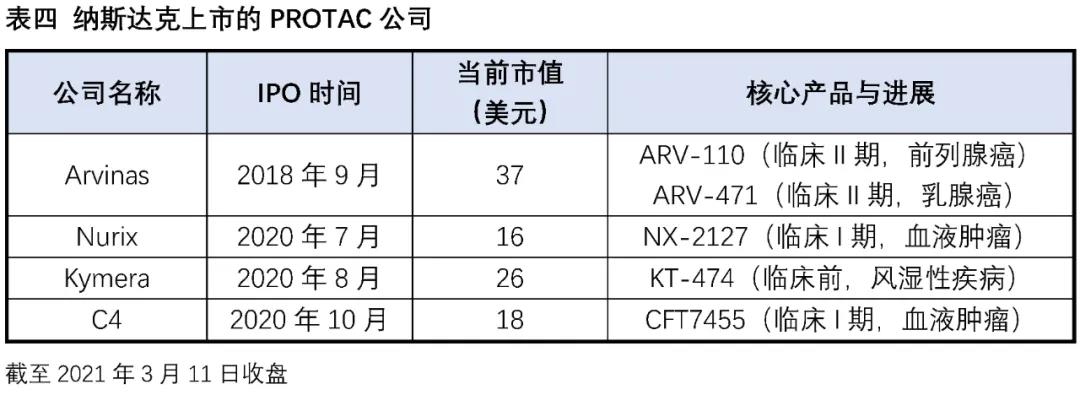 資料來(lái)源:WIND,康橙投資
資料來(lái)源:WIND,康橙投資
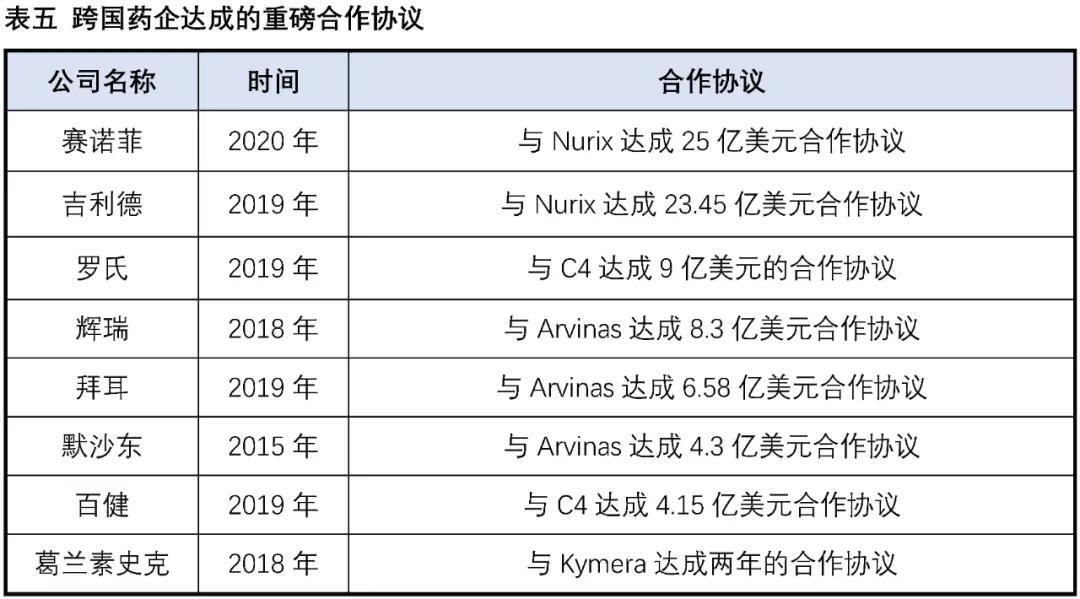
資料來(lái)源:康橙投資
2.分(fēn)子膠
分(fēn)子膠(Molecular Glues)是一類可(kě)以誘導或穩定蛋白質間相互作用(yòng)的(de)小分(fēn)子化(huà)合物(wù)。當其中一個(gè)蛋白質分(fēn)子爲泛素連接酶時(shí),分(fēn)子膠可(kě)以引起另外一個(gè)蛋白質發生泛素修飾,并通(tōng)過蛋白酶體途徑發生降解,與PROTAC有異曲同工之妙。經典的(de)分(fēn)子膠降解劑如沙利度胺類似物(wù)和(hé)芳基磺酰胺類抗癌藥Indisulam等都是利用(yòng)E3泛素連接酶與靶蛋白之間的(de)互補蛋白-蛋白作用(yòng)界面,重編程泛素連接酶的(de)選擇性,以催化(huà)劑的(de)方式驅動靶點泛素化(huà)。因此,分(fēn)子膠也(yě)巧妙地避開了(le)傳統抑制劑的(de)局限性,使得(de)一部分(fēn)靶點從“無成藥性”變爲“有成藥性”,同時(shí)分(fēn)子膠相比PROTAC有更小的(de)分(fēn)子量,理(lǐ)論上會有更好的(de)成藥性。早期發現的(de)分(fēn)子膠也(yě)多(duō)是偶然所得(de),近年來(lái)主動設計的(de)分(fēn)子膠也(yě)取得(de)了(le)不錯的(de)進展。2020年11月(yuè),禮來(lái)制藥與萬春醫藥子公司萬春Seed完成簽署總金額達到7.9億美(měi)元的(de)合作,将借助Seed自主研發的(de)獨特分(fēn)子膠蛋白降解專利技術開發候選新藥。2020年12月(yuè),分(fēn)子膠技術公司Neomorph宣布完成1.09億美(měi)元的(de)A輪融資,用(yòng)以推進專有的(de)靶向蛋白降解平台以及相關項目的(de)發展。同月(yuè),勃林(lín)格殷格翰也(yě)在分(fēn)子膠領域有所布局,與Proxygen簽訂了(le)合作和(hé)授權協議(yì),共同開發靶向多(duō)種緻癌靶點的(de)分(fēn)子膠降解劑。2021年3月(yuè),Monte Rosa Therapeutics宣布完成9500萬美(měi)元的(de)C輪融資用(yòng)于将其主要分(fēn)子膠産品推入臨床,加速管線發展并增強平台能力。
3. 變構調節
變構調節(Allosteric Regulation)通(tōng)過特異性影(yǐng)響蛋白構象變化(huà),從而将其穩定在某個(gè)非活化(huà)或活化(huà)狀态,這(zhè)與傳統的(de)底物(wù)競争性抑制劑比如ATP競争性激酶抑制劑有所不同。變構調節中有一個(gè)有趣的(de)“胖子理(lǐ)論”,以激酶抑制劑設計爲例,激酶底物(wù)比如ATP與酶活性中心結合緊密,就像是一個(gè)胖子坐(zuò)在一把椅子上。傳統的(de)競争性抑制劑要把這(zhè)個(gè)胖子拉起來(lái),需要更大(dà)的(de)力氣,也(yě)就是更高(gāo)的(de)親合力。而變構抑制劑則是在椅子的(de)某處紮了(le)一根釘子,胖子自己就跳起來(lái)了(le),并不需要多(duō)大(dà)的(de)力氣。變構調節因爲其“四兩撥千斤”的(de)獨特機制,不僅具有更好的(de)選擇性、安全性和(hé)克服耐藥的(de)潛力,還(hái)能使得(de)一部分(fēn)靶點從“無成藥性”變爲“有成藥性”,引起了(le)衆多(duō)科研機構和(hé)制藥企業的(de)重點關注。随著(zhe)結構生物(wù)學的(de)發展,變構位點的(de)确認變得(de)相對(duì)容易,也(yě)進一步推動了(le)變構調節小分(fēn)子藥物(wù)的(de)開發。
諾華的(de)BCR-ABL1變構抑制劑Asciminib,與BCR-ABL1蛋白的(de)肉豆蔻酰基位點結合(非ATP結構位點),通(tōng)過不同于其他(tā)BCR-ABL1激酶抑制劑的(de)機制将BCR-ABL1鎖定爲無活性構象。Asciminib在用(yòng)于曾接受過兩種以上酪氨酸激酶抑制劑(TKI)治療,并且對(duì)最近接受的(de)TKI治療産生耐藥性或不耐受的(de)慢(màn)性髓系白血病(CML)患者的(de)3期臨床試驗的(de)初步分(fēn)析中達到主要臨床終點,并于近期獲得(de)FDA授予的(de)2項突破性療法(Breakthrough Therapy)資格。最近兩年比較火熱(rè)的(de)KRAS抑制劑(如AMG510,臨床III期,已提交上市申請)、SHP2抑制劑(TNO155,臨床II期)都是相應靶點的(de)變構抑制劑,均是“不可(kě)成藥靶點”的(de)偉大(dà)突破。
4. 老藥新用(yòng)
“The best way to discover a new drug is to start with an old one”,這(zhè)是1988年諾貝爾生理(lǐ)學或醫學獎獲得(de)者藥理(lǐ)學家James Black提出的(de),簡而言之就是“老藥新用(yòng)”。“老藥”是指已上市的(de)藥物(wù)或正在進行臨床試驗的(de)藥物(wù),“新用(yòng)”是指發現在新的(de)适應症上使用(yòng)這(zhè)些藥物(wù)。
阿司匹林(lín)于1899年在美(měi)國被發明(míng),作爲解熱(rè)鎮痛藥的(de)應用(yòng)已有百餘年,随著(zhe)臨床研究的(de)不斷深入,阿司匹林(lín)的(de)許多(duō)新功效和(hé)新作用(yòng)逐漸被發現,特别是其心血管疾病預防和(hé)治療中的(de)作用(yòng)。《中國心血管病預防指南(nán)(2017)》中開始将低劑量阿司匹林(lín)作爲心血管疾病預防的(de)基礎藥物(wù)。臭名昭著的(de)沙利度胺同樣也(yě)是老藥新用(yòng)的(de)經典案例,20世紀50年代沙利度胺(商品名:反應停)成功在歐洲上市,在短短幾年時(shí)間裏就造成了(le)全球上萬例新生兒(ér)畸形(海豹胎),成爲藥物(wù)史上最大(dà)的(de)悲劇之一,使得(de)該藥品于1963年被迫退市。1964年醫生在給麻風病患者使用(yòng)時(shí),結果意外發現沙利度胺可(kě)以有效地減輕患者的(de)皮膚症狀。20世紀90年代又陸續發現了(le)抗炎、抗腫瘤作用(yòng),1998年沙利度胺被FDA批準用(yòng)于多(duō)發性骨髓瘤的(de)治療。西地那非(商品名:萬艾可(kě))最初開發是用(yòng)于擴張心血管平滑肌以擴張血管治療心絞痛,但是療效不盡人(rén)意,同樣的(de)作用(yòng)機制,臨床上發現其對(duì)陰莖海綿體平滑肌的(de)舒張作用(yòng)卻很顯著。1998年,FDA正式批準西地那非用(yòng)于勃起功能障礙治療。
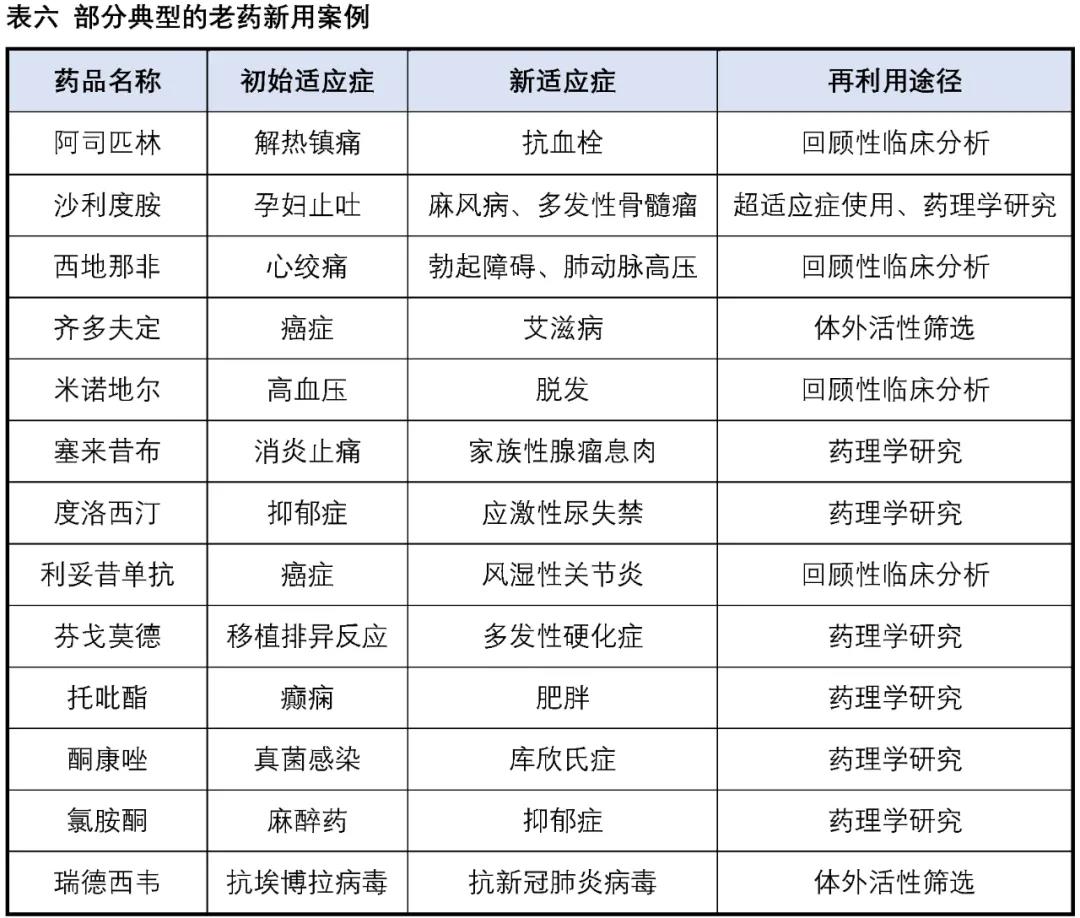
資料來(lái)源:康橙投資
過去幾十年裏,與阿司匹林(lín)、沙利度胺、西地那非等藥物(wù)一樣,“老藥”改變用(yòng)途成爲“新藥”的(de)成功案例也(yě)不在少數,爲患者與制藥公司都帶來(lái)不可(kě)估量的(de)獲益。2020新型冠狀病毒肺炎疫情中,“老藥新用(yòng)”也(yě)同樣發揮了(le)重要的(de)作用(yòng)。新冠疫情來(lái)得(de)非常突然,想要從頭設計獲得(de)一個(gè)全新的(de)抗新冠病毒藥物(wù)用(yòng)于疫情的(de)控制顯然是來(lái)不及的(de)。除了(le)抓緊研發新冠疫苗,也(yě)有非常多(duō)的(de)科學家希望能從現有的(de)上市的(de)或者進入臨床後期的(de)化(huà)合物(wù)中進行篩選,找到潛在的(de)新冠治療藥物(wù)。抗瘧藥如羟氯喹,抗病毒藥物(wù)如洛匹那韋、利托那韋、利巴韋林(lín)等,也(yě)包括了(le)“人(rén)民的(de)希望”-瑞德西韋都開展了(le)針對(duì)新冠的(de)臨床試驗。美(měi)國FDA于2020年5月(yuè)1日宣布授予瑞德西韋緊急使用(yòng)授權(EUA)治療COVID-19患者,雖然最後的(de)治療效果并不是那麽理(lǐ)想,但也(yě)爲阻止全球新冠疫情的(de)進一步惡化(huà)起到了(le)一定的(de)積極作用(yòng)。
在氘代藥物(wù)、共價抑制劑、多(duō)肽藥物(wù)等發展相對(duì)成熟的(de)技術方面,小分(fēn)子藥物(wù)也(yě)很有可(kě)能迎來(lái)突破。随著(zhe)人(rén)工智能(AI)技術的(de)不斷成熟以及在新藥研發中的(de)不斷滲透,人(rén)工智能在靶點發現、苗頭化(huà)合物(wù)與先導化(huà)合物(wù)發現、藥物(wù)分(fēn)子合成路線設計、疾病模型建立、新适應症挖掘等諸多(duō)方面助力新藥研發,将大(dà)大(dà)提高(gāo)新藥的(de)研發效率。近日,AI制藥巨頭強強聯合,Roivant拟以20.5億美(měi)元收購(gòu)Silicon Therapeutics(首付款4.5億美(měi)金+裏程碑付款);國内互聯網巨頭BAT(百度、阿裏、騰訊)近年來(lái)也(yě)投入大(dà)量精力積極布局AI藥物(wù)發現,相信借助人(rén)工智能技術不論是小分(fēn)子藥物(wù)還(hái)是大(dà)分(fēn)子藥物(wù)都能迎來(lái)蓬勃發展的(de)時(shí)機。小分(fēn)子藥物(wù)有其難以替代的(de)優勢,它的(de)發展也(yě)是困境與突破交替輪動的(de)曆史,随著(zhe)各種新科技的(de)不斷湧現,我們也(yě)期待能有更多(duō)的(de)“黑(hēi)科技”助力小分(fēn)子藥物(wù)研發的(de)突破,給世界帶來(lái)更多(duō)的(de)驚喜。
勇當主角,甘當配角。小分(fēn)子藥物(wù)在藥物(wù)發展史的(de)中一直擔任“主角”,随著(zhe)各種生物(wù)技術療法的(de)日益豐富與成熟,疾病的(de)治療手段必然會呈現百花齊放的(de)趨勢。近年來(lái)聯合用(yòng)藥也(yě)逐漸成爲臨床試驗發展的(de)趨勢,特别是腫瘤免疫療法的(de)興起,更是進一步推動了(le)聯合用(yòng)藥方案的(de)嘗試與突破。我想未來(lái)在某些疾病領域小分(fēn)子藥物(wù)依然會是“主角”,在另一些領域小分(fēn)子藥物(wù)可(kě)能真的(de)會逐步被取代直至淘汰,在更多(duō)的(de)領域将是小分(fēn)子藥物(wù)與生物(wù)技術療法的(de)“強強聯合”,從而更好地爲患者排憂解難。
----------THE END----------
免責聲明(míng):本文系轉載分(fēn)享,文章(zhāng)觀點、内容、圖片及版權歸原作者所有,如涉及侵權請聯系删除!